Gaz Klor ile Dezenfeksiyon
Gaz Klor ile Dezenfeksiyon
Hidrodos, gaz klorlama sistemleri dizaynı, tedariği ve anahtar teslim kurulumu konularında hizmet vermektedir.Gaz klorlama konusunda genel bilgiler için aşağıdaki makaleye göz atabilirsiniz.
 | Diğer Detaylarla ilgili Yardımcı Linkler için : Gaz klorlama sisteminde kullanılan ürünler - Tank odasında bulunan ekipmanlar - Klorinatör odasında bulunan ekipmanlar - Koruyucu elbise ve ekipmanlar - Kontrol ve gözlem odası ekipmanları Gaz klorlama sistemi dizaynı için soru föyü | ||||||||||||||
KLOR KİMYASI İLE İLGİLİ GENEL BİLGİLENDİRMELERKLOR NEDİR?Klor 90 doğal elementten biridir. Yüksek oranda reaktiftir ve doğada diğer elementlere bağlı olarak bulunur. Örneğin Sodyum ile birleşerek sofra tuzu dediğimiz sodyum klorür'ü oluşturur.Klor birçok uygulamada önemli bir rol üstlenir: - İçmesuyunda kolera ve tifo gibi hastalık yapıcı bakteri ve virüslerin kontrolünde kullanılır. Modern içmesuyu arıtma tesislerinin %98'inde klor ile dezenfeksiyon yapılmaktadır. - İlaç endüstrisinde %90 oranda ilacın üretiminde klor kullanılır. Bu ilaçlar kalp hastalıkları, kanser, AIDS ve diğer hayatı tehdit eden hastalıklar için kullanılmaktadır. - Klor tahılların üretiminde diğer koruyucu kimyasallara göre %96 oranında kullanılmaktadır. KLORUN ÜRETİMİKlorun üretiminde elektrolitik diyafram, membran ya da civa hücresi prosesleri kullanılır. Her bir proseste tuz solusyonu (salamura) (sodyum ya da potasyum klorür) doğrudan elektrik akımı altında elektrolize uğrar. Bu işlem sonucunda klorür iyonları element halindeki klora (Cl2) dönüşürler.Klor birçok başka yöntemle de üretilebilmektedir. Örneğin erimiş tuzun ya da magnezyum klorürün elektrolizi ile element halinde sodyum veya magnezyum metali oluşturarak, Hidroklorik asitin elektrolizi ile ve elektrolitik olmayan proseslerle. En basit klor alkali kimyasal reaksiyonu aşağıdaki gibi özetlenebilir: Tuz + Su + Elektrik → Klor + Kostik + Hidrojen NaCl+ H2 O + e− → 1/2Cl2 + NaOH +1/2 H2 Diyafram Hücre Teknolojisi ile klor ve hidrojen gazı üretilebilir. Ek ürün olarak sodyum hidroksit ve sodyum klorür solusyonu oluşur. Ürün %16lık sodyum klorürdür ve buharlaştırma prosesleri ile %50 lik konsantrasyona çıkarılabilir. Membran Hücre Teknolojisinde iyon değiştirici (katyon seçici) membranlar kullanılarak anot ve katotlarda oluşan ürünler ayrılır. Son ürün olarak anot bölümünde klorür iyonlarından klor gazı, katot bölümünde ise su, hidrojen gazı ve hidroksit iyonlarına indirgenir. Membranın topladığı sodyum iyonları ile hidroksit iyonları birleşerek sodyum hidroksiti oluşturur. Ürün %30 -35 lık sodyum hidroksittir ve buharlaştırma yöntemi ile %50 lik konsantrasyona çıkarılabilir. Civa Hücresi Teknolojisinde katot olarak elektrolizörün altından civa akar. Anotlar paralel olarak hücre içinde akan civanın milimetrik mesafede üzerinde asılıdır. Salamura sisteme verildiğinde yerçekimi ile anot ve katotların arasından geçerken anot üzerine klor gazı oluşur. Sodyum iyonları civa katot üzerinde birikirler. Bu sistemde %50 sodyum hidroksit ve hidrojen üretilir. KLORUN TAŞINMASI Klor normalde basınç altında sıvılaştırılmış gaz olarak taşınır. Tehlike sınıfı Birincil olarak 2, İkincil olarak 5,8 kodu ile zehirli gaz, oksitleyici ve korozif olarak tanımlanmıştır. Amerika ve Kanada'da Kara yolları taşıma yönetmeliği 49 CFR, 46 CFR, 33 CFR ve Zone B sınıfında solunması tehlikeli madde olarak belirtilmektedir. Uluslararası karayolları şartlarına göre TDG ve IMDG ve taşınan kimyasal UN1027 kodu ile tanımlanmaktadır. ELEMENT HALİNDELİ KLOR Sembolü : Cl Atomik ağırlığı : 34,453 Atomik numarası : 17 Element klor Cl2 formunda iki klor atomundan oluşur. Molekül ağırlığı : 70,906 CAS başvuru numarası : 7782-50-5 SIVI KLOR Cl2'un soğutulmuş ve sıkıştırılmış formudur. Atmosferik sıcaklıkta ve basınçta sıvı klor hızlıca buharlaşır ve 1 pound sıvı klor 5.4 feet3 klor gazı oluşturur. (1 pound = 0.45 kg) (5.4 feet 3 =152 litre) (1 kg - 337 litre) Sıvı klor tanımı, hipoklorit veya sodyum hipoklorit solusyonları anlamına gelmez. GAZ KLOR Atmosferik şartlarda klor gaz formundadır. KURU KLOR (DRY)/ NEM İÇEREN (WET) KLOR Kuru klor (sıvı yada gaz), içinde nem oranı ayrı bir faz oluşturmayacak ve suyun serbest hale geçmeyecek kadar düşük olan klordur. Su tamamen klor içinde çözünmüştür. Eğer bu solusyonun içindeki nem içeriği artar ise solusyon içinde su ikinci bir faz oluşturur ve serbest kalır, bu durumdaki klora (sıvı ya da gaz) Nem içeren klor denir. Nem içeren klor korozyon oluşturacak bileşenler yaratarak sistemin güvenliğini ve bütünlüğünü tehlikeye atar. Aşağıdaki eğride suyun sıvı klor içinde çözündüğü durumlar sıcaklığa bağlı olarak görülebilir. 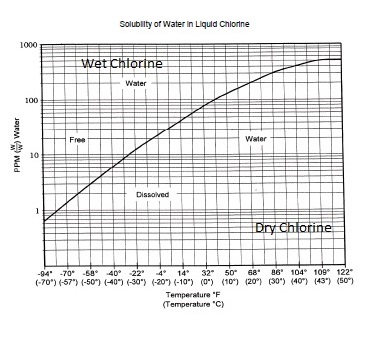 Burada görülebileceği gibi 10oC sıcaklıkta 30 ppm su içerikli klor kurudur. Eğer sıcaklık -20oC ye düşerse klor artık nemli (wet) forma geçecektir. 5oC sıcaklıkta su içeriği 100 ppm değerini aşmadığı sürece klor kuru formdadır. Kuru klor tanımı, kalsiyum hipoklorit gibi kuru klorlu bir bileşik olarak anlaşılmamalıdır. KLOR SOLUSYONU Sudaki klor solusyonudur. Klor solusyonu hipoklorit ya da sodyum hipoklorit (NaOCl) ile karıştırılmamalı ve aynı anlamda kullanılmamalıdır. DOLDURMA YOĞUNLUĞU Klorun tanklara doldurulması sırasında yoğunluğunun 60°F (15.6°C) de suyun %125 'inden fazla olmaması istenir. SODYUM HİDROKSİT Sodyum hidoksit (NaOH), klor üretilirken sodyum klorür solusyonunun elektroliz işlemi sırasında tüketimi ile ortaya çıkan bir yan üründür. Kostik soda da denmektedir. Klor gazı yanıcı ya da patlayıcı değildir ancak belirli oranlarda hidrojen ile karıştırılğında ya da azottriklor ile bir araya geldiğinde yanıcı ve patlayıcı özellik kazanır. Bazı durumlarda klor yanmayı hızlandırır. Klor birçok maddeye karşı yüksek kimyasal afinite gösterir. Birçok inorganik ve organik bileşik ile reaksiyona girer, bu reaksiyon sonucunda ısı açığa çıkar. Uygun şartlar altında klor, bazı metaller ile de reaksiyon gösterebilir. Ortam sıcaklıklarında kuru klor (sıvı ya da gaz formunda) çeliğe korozyon etkisi göstermez. Nem içeren klor ise yüksek oranda koroziftir çünkü hidroklorik ve hipokloröz asidi oluşturur. Kloru ve klor ekipmanlarını kuru tutmak için gerekli önlemler alınmalıdır. Boru, vana ve tankların kullanılmadığı zamanlarda uygun bir şekilde kapatılması ve atmosferik nemin sistem içine girmemesi sağlanmalıdır. Klor kaçakları sırasında su kullanılacak ise kaçak olan yerdeki korozyonun daha da ilerleyeceği unutulmamalıdır. Sıvı klorun hacmi sıcaklık ile artar. Sıvı klor ile dolu boru, tank vb kapalı kapların hidrostatik parçalanmasına karşı gerekli önlemler alınmalıdır. SİLİNDİRLER Klor silindirleri çekme çelik malzemeden 1-150 lb (0.45-68 kg) kapasitelerinde imal edilmektedir. En çok bulunanları 45.4 ve 68 kg (100 - 150 lb) olanlarıdır. Silindir üzerindeki tek bağlantı bulunur, bu kısımda klor vanası yer alır. Çelik vana taşıma ve depolama sırasında koruyucu kapağı ile birlikte tutulmalıdır. Silindirler dikey olarak kullanılırlar. TONLUK TANKLAR Tonluk tanklar 2000lb (907 kg) kapasitelidirler. En çok 3650 lb (1655kg) doldurulabilirler. Her iki ucunda kaldırma kirişi ile taşınabilmesi için uzantıları vardır. Tonluk tankların iki adet vanası bulunur. Bu vanalar da kullanılmadığı durumda koruyucu kapak ile koruma altında bulundurulmaldıır. Tonluk tanklar yatay olarak kullanılırlar. Taşınması ve vanaların düzgün konumda yerleştirilmesi için kreyn sisemi ve mesnet tekerleri kullanılır. TANKLARDAN GAZ KLOR DEŞARJI Klor gazı deşarj oranları lokal ortam sıcaklığı, nem ve hava sirkülasyonundan önemli oranda etkilenir. Bir tanktan alınan kapasite yeterli olmuyor ise birkaç tankın kollektöre bağlanması önerilir. Kollektörler kullanılıyor ise tüm tankların aynı sıcaklıkta olması sağlanmalıdır. Bir tankın sıcaklığı diğerinden farklı ise gaz transferi nedeniyle diğer tankın sıcaklığında düşme yaşanabilir. TANKLARDAN SIVI KLOR DEŞARJI Sıvı klor tonluk tankın altta kalan vanasından alınabilir. Bu ancak çok yüksek oranda klor gereksinimi olduğunda tercih edilmelidir. Deşarj hızı tonluk tankın içindeki klorun sıcaklığına ve karşı basınca bağlıdır. Normal şartlar altında ve 35 psi (2.41 bar) karşı basınç var ise tanktan en az 40 lb/saat (181 kg/saat) kapasite ile sıvı klor alınabilir. Kollektöre bağlandığında tonluk tankların basınç dengelenmesi konusunda önlem alınması gereklidir. Borulamada ise sıvı klorun hatlarda sıkışmadığından emin olunması gereklidir. AĞIRLIK Klor basınç altında sıvılaştırılmış gaz olarak taşındığından tank içindeki basınç klorun sıcaklığına bağlıdır. Basınç tank içindeki klorun miktarına bağlı değildir. Tankta ne kadar klor olduğu sadece tartılarak belirlenebilir. 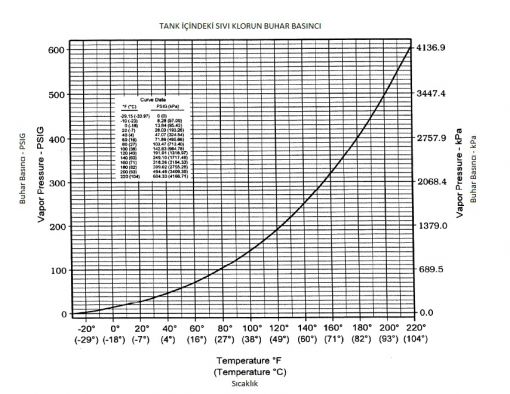 Bir tank içindeki sıvı klorun sıcaklıkla hacmindeki değişim ise aşağıdaki gibidir. 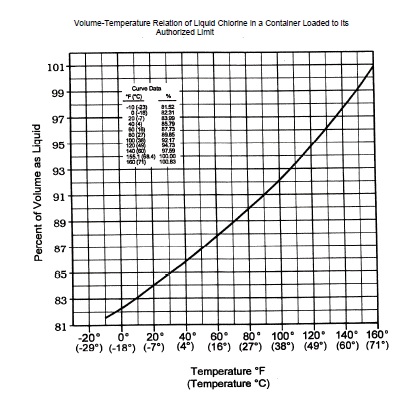 Klor tankından çekilen klor, gaz klor formunda kaldıkça bir problem yaratmaz. Ancak borularda ve sistemde sıcaklık kaybı olduğunda klor sıvılaşacak ve sıcaklık aynı derecelerde kaldıkça tekrar gaza dönüşemeyecektir. Bu sıvılaşmayı engellemek için sistemin hiçbir zaman soğuk bölgelerden geçmemesi, gece zamanlarında açık pencereler bulundurulmaması sağlanmalıdır. Herhangi bir sıcaklıkta yukarıda bahsedilen sıvılaşma gerçekleşebilir. Hatların sıcaklığı her zaman tank sıcaklığından yüksek olmalıdır. Örneğin : Bir tanktan çekilen gaz 30C sıcaklıkta ise sıvı klora 28C sıcaklıkta dönüşecektir. BAĞLANTILAR Tanklar ile kollektörün bağlantısı klora uygun esnek bağlantılar ile yapılmalıdır. Eğer sistem tanklar bağlıyken veya değiştirilirken çalışır durumda olacak ise yardımcı izolasyon vanaları kullanılmalıdır. Esnek bağlantılar düzenli olarak kontrol edilmeli ve değiştirilmelidir. Bağlantı contası da her tank değişiminde yenisi ile değiştirilmelidir. TANK VANALARI İşletmeye alırken tank vanalarının saat yönünün tersine bir tur döndürülmesi yeterlidir. Tank vanalarını açarken anahtarlar kullanılmalıdır ve anahtar tank üzerinde bırakılmalıdır ki acil durumda tank vanası hemen kapatılabilsin. Devreye alma sırasında tank vanasının çeyrek tur açılması yeterlidir. Kaçakların tespitinden ve giderilmesinden sonra tank vanası yukarıda belirtildiği gibi bir tur açılabilir. TANKLARIN DEĞİŞTİRİLMESİ Bir tank boşaldı ise vanaları kapatılmalı, tamamen sökülmeden önce esnek bağlantı içindeki birikmiş klorun da vakum ile çekilmesi beklenmelidir. Her olasılığa karşı emniyet kıyafetleri (PPA) giyilmiş olmalı ve daha sonra tank, bağlantılarından tamamen sökülmelidir. Kullanılmayacak tankların üzerine koruyucu kapakları geçirilmeli ve boş tank alanında saklanmalıdır. Açık kalan esnek bağlantı ucuna uygun şekilde izolasyon yapılmalı ve sisteme atmosferik nem girmesi engellenmelidir. NÖTRALİZASYON SİSTEMLERİ Klor, alkali bir solusyon ile hemen reaksiyona girer ve bu şekilde absorbe edilebilir. Su ve sodyum hidroksit, sodyum karbonat, potasyum hidroksit gibi bir solusyon ile bu işlem gerçekleştirilebilir. KLOR TEMAS EŞİKLERİ ve BELİRTİLER
KLOR SİSTEMLERİ İÇİN BORULAMA Genel olarak klor (dry/kuru) sistemlerinde proses sıcaklığı -29 ile 149C arasında ise ASTM A106 Gr B Sch 80 çekme çelik karbon borulama kullanılır. Paslanmaz çelik 300 serisi düşük sıcaklıklarda kullanılabilir ancak klor stresi ile korozyon kırılmaları görülebilir. Nem içeren ortamlarda ve değişkenlik gösteren sıcaklık koşullarında bu durum sıklıkla yaşanır. Titanyum, aluminyum, altın, kalay, kuru klor (dry chlorine) ile kullanılamaz. Klor uygulamasında bazı plastikler kullanılmamalıdır. Mutlaka periyodik olarak sistemin gözlenmesi gerekmektedir. Sıvı klor için ise malzemeler çok dikkatlice seçilmelidir. Sıvı klor oldukça koroziftir ve birçok inşaat malzemesine zarar verir. Düşük basınçlarda sıvı klor kimyasal betonu, cam ya da porselen gibi malzemelerle taşınmalıdır. Sert plastik , plastik içermeyen polivinil klorür, cam takviyesi ile güçlendirilmiş polyester, polivinil klorür ya da florür reçineler kullanılması önerilir. Yüksek basınçlarda Hastelloy C, titanyum ve tantalum kullanılabilir. Titanyum sadece nemli klor ile kullanılabilir, kuru klor ile kullanılmamalıdır. Kuru klor ile kullanıldığı durumlarda hemen yanar. Tantalum ise nemli ve kuru klor ile 149oC sıcaklığa kadar kullanılabilir. KİMYASAL ÖZELLİKLER Sıvı klorun buharlaşma noktası Sıvılaşma - kaynama noktası : -29,15oF (-33,97oC)@101,325kPa Katı klorun eridiği ya da sıvı klorun katılaştığı nokta Sıvı klorun erime - donma noktası : -149,76oF (-100,98oC) Kritik basınç ve sıcaklıkta bir hacim klorun kütlesi Kritik Yoğunluğu : 573,0 kg/m3 Kritik sıcaklıkta sıvı klorun buhar basıncı Kritik Basınç : 7977 kPA Basınçtan bağımsız olarak klorun sadece gaz formunda olmaya başladığı sıcaklık. Kritik Sıcaklık : 143,75oC Kritik basınç ve sıcaklıkta bir birim kütledeki klorun hacmi Kritik Hacim : 0,001745 m3/kg Özel sıcaklık ve basınç şartları altında birim hacimdeki klorun kütlesi Yoğunluk Klor gazının yoğunluğu : 3,213 kg/m3 @0oC 101,325 kPa Doymuş Klor gazının yoğunluğu : 12,23 kg/m3 @0oC 368,9 kPa Sıvı - gaz hacim ilişkisi Bir hacim sıvı klorun ağırlığı 456,5 hacim klor gazının ağırlığına eşittir. @0oC 101,325 kPa WSıvı klor = 456,5 x WGaz Klor KLOR KİMYASI Klor suda %0,3 - %0,7 oranlarında çözünebilir. Bu oran suyun sıcaklığına bağlıdır. Klor gazı suda aşağıdaki tepkimeye göre davranarak oksidasyon ve dezenfeksiyonu sağlayıcı Hipoklorit iyonlarını oluşturur: | |||||||||||||||
| Hipoklorit iyonlarının oluşumu aşağıdaki eğride görüldüğü gibi pH değerinden etkilenir, bu nedenle dezenfeksiyon uygulamalarında çok daha etkili bir sonuç alabilmek için pH değerinin alkali olması gerekmektedir. Benzer şekilde klor gazı artan sıcaklık ile çözünürlüğünü yitirecektir. Bu sebeple gün - ay ve yıl boyunca tesise gelen suyun sıcaklığına göre işletme personeli, klor dozaj değerini sıcaklık faktörünü göz önünde bulundurarak düzenlemelidir. 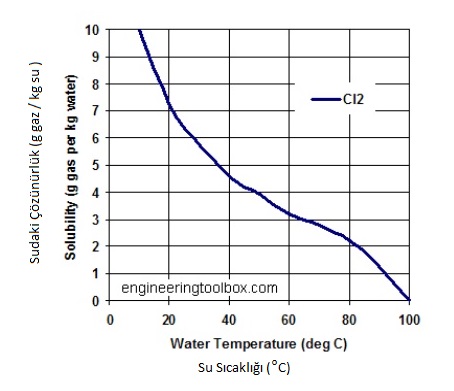 | |||||||||||||||
| Suda amonyak içeriği var ise veya atıksu uygulamalarında klor ile dezenfeksiyon sırasında kloraminler oluşur. Bu durumdaki klora bağlı klor denilmektedir ve bu şekli ile klor dezenfeksiyonunda kullanılamaz. Bu nedenle öncelikle amonyak içeriğinin oksidasyonu yapılmalı ve sonrasında dezenfeksiyon için yeterli oranda klor bakiyesi kalana kadar (kırılma noktası klorlaması esaslarına göre) klorlama işlemine devam edilmelidir. Atıksuda bulunan toplam koliform sayısına göre istenen toplam klor bakiyesi ile ilgili tabloyu aşağıda bulabilirsiniz: 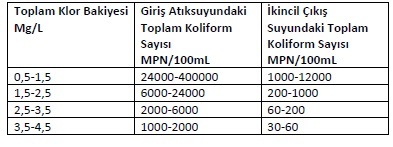 OKAS kodu:klorlama donanımı 42993100 | |||||||||||||||






